《退市意见》或波及长生生物,“公众健康”成上市公司新红线
昨日,证监会主席刘士余签发新令,对2014年《关于改革完善并严格实施上市公司退市制度的若干意见》(以下简称《退市意见》)进行修改。上市公司重大违法强制退市制度由“先暂停上市后终止上市”升格为“可暂停上市,也可直接停止上市”。且《退市意见》或将波及深陷违法生产狂犬病疫苗案件的长生生物。
健康点healthpoint - 退市意见,公众健康 - 2018-07-28
2024 FDA指南:新药上市协议和ANDA标签中成分声明的内容和格式
本指南旨在帮助新药申请(NDA)和简化新药申请(ANDA)申请人在其申请中提交准确、完整的成分声明,并在标签中提交相应的成分声明(如适用)。本指南介绍了在标签中编写成分声明和相应成分声明的最佳实践。
FDA官网 - 新药上市 - 2024-05-02
无营收生物企业拟赴港上市 歌礼生物“首吃螃蟹”
港交所修订后的主板上市规则生效7天后,首个“吃螃蟹”的企业浮出水面。5月7日,歌礼生物(Ascletis Pharma Inc.)正式向港交所提交上市申请,成为第一家利用新规则赴港上市的尚未盈利的中国大陆生物科技公司。
健康界 - 生物企业 - 2018-05-09
原研药索非布韦有望18年初在国内上市
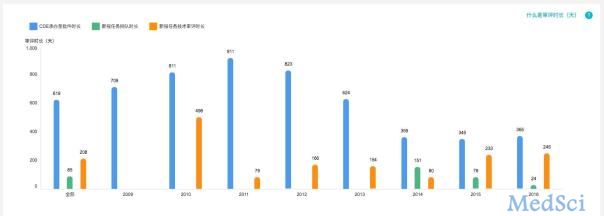
的集中审评和审评人员增加,加速了中国药物审评的速度,但进口药物却从 2014 年开始经历三报三批流程的申报流程,这一并无明文规定的进口药审评潜规则,使得本来不管在患者、市场,还是外资药企中,已经诟病已久的对原研药在中国的上市时间比国际市场上市时间晚的问题更加严重
Insight数据库 - 索非布韦 - 2017-03-20
原研尚未获批 ED药物阿伐那非国内首款上市
日前,海思科发布公告称,其按照注册分类3(境内申请人仿制境外上市但原研未在境内上市)申报的阿伐那非片已获得国家药监局颁发的《药品注册证书)(批准文号:国药准字H20213212 、国药准字H20213
医谷网 - 阿伐那非,恒瑞医药, ED药物 - 2021-04-03
国药集团提交新冠疫苗上市申请,全球其他新冠疫苗进展如何?
中国国药集团有限公司副总经理石晟怡日前表示,中国国药集团已向国家药监局提交了新冠疫苗上市申请。
医谷网 - 受试者,新冠疫苗,竞争对手 - 2020-12-03
儿童顽固“湿疹”可能是特应性皮炎 非激素用药正式上市
据统计,在我国约有7000-9000万特应性皮炎患者,其中中重度患者占到了30%,由剧烈瘙痒引起的睡眠缺失及心理问题严重影响着患者生活质量,同时也给患者家庭和社会带来巨大的经济负担。
39健康网 - 特应性皮炎 - 2020-10-15
干细胞药物上市迈出了一大步
近日,国内以药品形式申报的干细胞治疗产品的新药临床试验申请(IND)获得了批准,意味着我国干细胞药物上市迈出了一大步。也就是说,国内患者能够使用上干细胞药物的日子越来越近了。
博雅干细胞 - 干细胞,细胞治疗,临床试验 - 2019-01-22
美罗华再迎新对手,第二款国产利妥昔单抗上市
昨日(10月9日),据国家药监局官网数据显示,信达生物的利妥昔单抗注射液(商品民:达伯华)获批上市,根据信达生物发布的公告,该药将用于治疗弥漫性大B细胞淋巴瘤、滤泡性淋巴瘤及慢性淋巴细胞性白血病,这也
医谷网 - 美罗华,利妥昔,考核制度 - 2020-10-10
第二个国产三代EGFR-TKI获批上市
据国家药监局官网最新消息,艾力斯的核心产品——不可逆、高选择性第三代EGFR抑制剂甲磺酸伏美替尼片获批上市,该产品是目前市面上获批上市的第三个第三代EGFR-TKI,也是艾力斯
医谷网 - 药物,EGFR-TKI,获批上市 - 2021-03-07
四价HPV疫苗上市遭“抢” 市场规模有望超过300亿
四价HPV疫苗自上市以来备受市场追捧,有券商预测,四价疫苗市场规模有望超过300亿元人民币。
北京青年报 - 四价,HPV疫苗 - 2017-12-18
Nature:新型丙肝口服药物获批上市 人类将首次战胜HCV
改进的治疗方案将为人类清除肝病毒感染提供新希望。 数十年来,丙型肝炎病毒(HCV)感染者都不得不忍受令人饱受折磨的治疗方案,其中包括注射干扰素药物,它可以引起严重恶心及抑郁症。随着几种高效口服抗病毒药物即将获得批准,以及更多药物的出现,研究人员说根除全世界的感染现在成为了一个现实的目标。 不同于以往的 HCV 治疗采用干扰素和其他药物来寻求增强免疫系统,最新的一组口服药物可以干扰病毒的复制
生物360 - 丙肝,口服药物,HCV - 2013-11-05
GSK/Genmab向FDA提交Arzerra作为CLL一线用药的上市申请
葛兰素史克与Genmab公司在美国提交了慢性淋巴细胞性白血病(CLL)药物Arzerra用于一线治疗的申请后,他们在扩大这款药物的适用范围上又迈出了一步。这两家合作伙伴向FDA提交了一份申请,寻求批准Arzerra (ofatumumab)用于之前未接受过治疗及不能接受以氟达拉滨为基础治疗的CLL患者。上个月,Arzerra的这一适应症被FDA授予突破性治疗药物资格。在临床试验中,以Arzerra
丁香园 - Arzerra,CLL,GSK - 2013-11-06
赛诺菲多发性硬化症新药Lemtrada获FDA批准上市
上周五,美国FDA更改了其早前的决定,决定批准制药巨头赛诺菲公司开发的多发性硬化症药物Lemtrada上市。这一决定也表明赛诺菲公司在这一领域再下一城。不过,和其他多发性硬化症药物类似,Lemtrada上市时,也会着重标明这种药物可能会导致自身免疫反应以及其他严重的不良反应。同时药物的使用有增大患者患甲状腺癌等恶性癌症的风险。
生物谷 - 赛诺菲,新药Lemtrada - 2014-11-19
为您找到相关结果约500个