百济神州宣布,百悦泽®(泽布替尼)获准用于治疗套细胞淋巴瘤患者
2021-10-13 国际文传 网络
这是百悦泽在澳大利亚通过审批的第二个适应证,紧随该药物最近首次在澳获准用于治疗华氏巨球蛋白血症
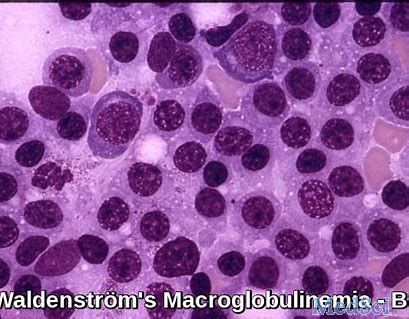
百济神州(BeiGene, NASDAQ: BGNE; HKEX: 06160)是一家全球性科学驱动型生物技术公司,专注于开发创新平价药物,以改善各国患者的治疗转归和药物可及性。该公司今天宣布,百悦泽(BRUKINSA®,泽布替尼)已在澳大利亚获准用于治疗既往接受过至少一种治疗药物的套细胞淋巴瘤(MCL)成人患者。2021年10月7日,百悦泽在澳大利亚首次通过审批,用于治疗既往接受过至少一种治疗药物的华氏巨球蛋白血症(Waldenström’s macroglobulinemia, WM)成人患者,或作为不适用化学免疫治疗药物患者的一线治疗药物1。
百悦泽已在澳获准用于两种适应证,随着该药在澳洲药物管理局(Therapeutic Goods Administration, TGA)的相关注册工作完成,上述患者将通过百济神州赞助的核准后、报销前获药项目立即获得百悦泽。
Monash Health临床血液科主任、泽布替尼临床试验主要研究者Stephen Opat教授表示:“套细胞淋巴瘤是一种非常见型非霍奇金淋巴瘤,一般认为无法治愈。虽然大多数患者初次治疗后缓解良好,但随着时间推移,几乎所有患者都将发展为进行性淋巴瘤。现有治疗药物对复发或难治MCL患者通常无效或因副作用而导致治疗中断。让我感到鼓舞的是,高选择性BTK抑制剂泽布替尼在两项针对复发或难治MCL的试验中取得了有令人满意的临床结果,该药将为澳大利亚的此类患者提供新的治疗选择。”
Lymphoma Australia首席执行官Sharon Winton表示:“澳大利亚是世界上非霍奇金淋巴瘤患病率最高的国家之一,此类患者需要现有治疗方法之外的新选择。百济神州通过赞助报销前项目为广大患者提供了获得百悦泽的机会,此举必将受到MCL患者的欢迎,因为新的治疗药物至关重要,特别是对于那些老年期获诊患者,因为老年人可能难以耐受一些较为剧烈的治疗方法。”
2021年7月,百济神州向药品保险咨询委员会(Pharmaceutical Benefits Advisory Committee, PBAC)提交百悦泽报销申请,寻求将MCL适应证纳入目录。
百济神州血液部首席医学官Jane Huang, M.D.表示:“百悦泽旨在提供深度而持久的缓解,同时减少脱靶副作用,以改善第一代BTK抑制剂的疗效。在百悦泽向TGA注册用于治疗WM并获批之后,我们立即启动了该药物在澳大利亚的早期临床试验,我们很高兴能向更多需要新治疗选择的澳大利亚患者提供百悦泽。”
在澳大利亚,每年有6,000多人确诊为非霍奇金淋巴瘤(NHL),在成人常见癌症中排名第六2。MCL是一种B细胞NHL,发生于称为套区的淋巴结外缘3。MCL通常预后较差,中位生存期介于3至6年,确诊时常已处于疾病晚期3。
百悦泽在澳大利亚注册用于治疗MCL的依据是两项单臂临床试验的有效性结果。在这两项试验中,根据独立评审委员会(IRC)按2014年卢加诺分类的评估,百悦泽总缓解率(ORR)达到83.7%,ORR定义为完全缓解(CR)和部分缓解(PR)的加总率。
泽布替尼治疗复发或难治(R/R) MCL患者多中心2期试验BGB-3111-206 (NCT03206970)中,中位随访时间为18.4个月,ORR为83.7% (95% CI: 74.2, 90.8),包括68.6%的CR(要求FDG-PET扫描)和15.1%的PR;中位缓解持续时间(DoR)为19.5个月(95% CI: 16.6, NE)。全球1/2期试验BGB-3111-AU-003 (NCT02343120)中,中位随访时间为14.75个月,ORR为84.4% (95% CI: 67.2, 94.7),包括25.0%的CR(未要求FDG-PET扫描)和59.4%的PR;中位DoR为18.5个月(95% CI: 12.6, NE)。
既往接受过至少一种治疗药物并接受百悦泽治疗的118例MCL患者中,13.6%的患者因试验中的不良事件而停止治疗,最常见的不良事件为肺炎(3.4%)。导致减低剂量的不良事件见于3.4%的患者,包括乙型肝炎、中性粒细胞减少、过敏性皮炎和周围感觉神经病变(各1例)。
百悦泽的总体安全性基于临床试验中接受百悦泽治疗的779例B细胞恶性肿瘤患者的汇总数据。百悦泽最常见的不良反应(≥20%)包括中性粒细胞减少、血小板减少、上呼吸道感染、出血/血肿、皮疹、瘀青、贫血、肌肉骨骼疼痛、腹泻、肺炎和咳嗽。最常见的3度或更高级别的不良反应(≥5%)为中性粒细胞减少、血小板减少、肺炎和贫血。
百悦泽推荐剂量为:单次160毫克每日2次或单次320毫克每日一次,口服,饭前或饭后均可服用。可根据不良反应调整剂量,重度肝功能损害及合用某些药物的患者可减低剂量。
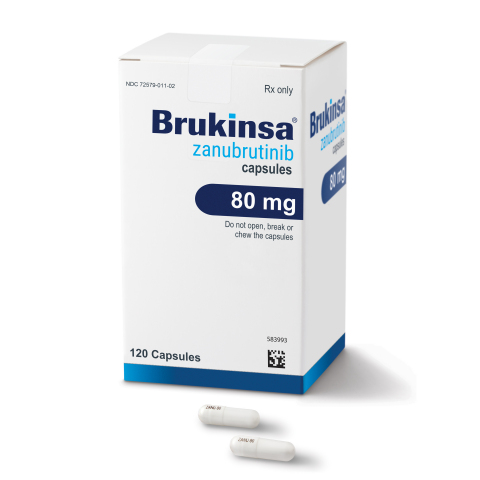
关于百悦泽®(泽布替尼)
百悦泽是百济神州科学家发现的布鲁顿酪氨酸激酶(BTK)的小分子抑制剂,全球多项临床研究目前正在评估其单独及联合其他药物用于治疗各种B细胞恶性肿瘤的效果。由于新的BTK不断合成,百悦泽经针对性设计,通过优化生物利用度、半衰期和选择性,可彻底而持久地抑制BTK蛋白。与其他获准的BTK抑制剂相比,百悦泽具有区分性的药代动力学特性,研究显示可抑制数种疾病相关组织内恶性B细胞的增殖。
百悦泽已在美国、中国、澳大利亚、加拿大和其他国际市场获准用于部分适应证,目前正在针对全球其他国家的报批进行开发。
百济神州肿瘤部
百济神州致力于促进血液学、免疫肿瘤学和靶向治疗,向全球患者提供有效平价药品。我们拥有约2,300名同事组成的不断壮大的研发团队,致力于推进90多项临床试验,涉及13,000多例患者和健康受试者。我们广泛的产品阵容由以内部为主的临床开发团队指导研发,正在40多个国家或地区进行试验。我们目前市售自有实验室发现和开发的三款药品:BTK抑制剂百悦泽(美国、中国、加拿大和其他国际市场);非FC-γ受体结合抗PD-1抗体替雷利珠单抗(中国);以及PARP抑制剂帕米帕利(中国)。百济神州拥有优质创新的科学和医学组织,是中国市场上的领先者,拥有专注于肿瘤学的大规模商业团队。
百济神州还积极与创新型公司合作。这些公司与我们拥有相同的目标,即开发治疗药物以满足全球健康所需。我们在中国市场对一系列安进和百时美施贵宝转让的肿瘤药物进行了商业化。我们还计划通过与安进、Bio-Thera、EUSA Pharma、Mirati Therapeutics、Seagen和Zymeworks等公司的合作,满足全球更大的未获满足的需求领域。百济神州还与诺华达成合作,向诺华转让在北美、欧洲和日本开发、制造和商业化替雷利珠单抗的权益。
(照片:美国商业资讯)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#细胞淋巴瘤#
49