2024 FDA指南:新药上市协议和ANDA标签中成分声明的内容和格式
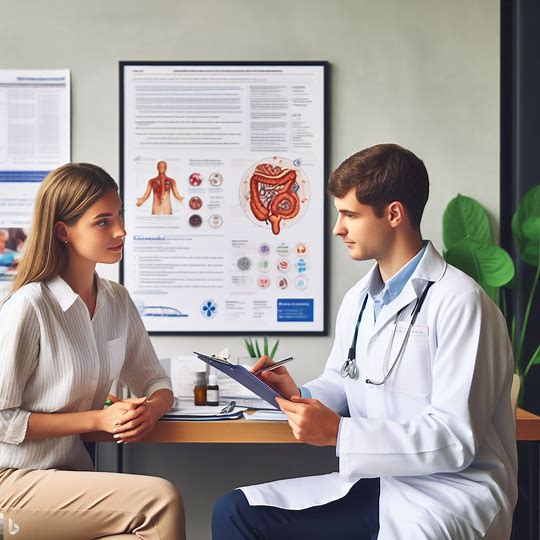
本指南旨在帮助新药申请(NDA)和简化新药申请(ANDA)申请人在其申请中提交准确、完整的成分声明,并在标签中提交相应的成分声明(如适用)。本指南介绍了在标签中编写成分声明和相应成分声明的最佳实践。
2024 FDA指南:处方生物参考品和生物仿制药的促销标签和广告注意事项 行业问答指南
本指南讨论了在这些促销信息中提供有关参考产品或生物仿制药的数据和信息的注意事项,以帮助确保它们准确、真实且无误导性。
2024 FDA指南:癌症临床试验资格标准:清除期和伴随药物
本指南是一系列指南之一,这些指南就 CDER 和 CBER 监管的用于治疗癌症的研究药物或生物制品的临床试验的资格标准提供了建议。具体而言,该指南包括有关适当使用清除期和同时排除药物的建议。
中国新药注册临床试验进展年度报告 (2023年)
国家药监局药品审评中心对 2023 年中国新药注册临床试验现状进行全面汇总和分析,同时对近年来的变化趋势特点进行分析,运用信息化手段助力提升临床试验安全监管能力。